11 июня 2026
Вы здесь
«Органы-призраки» для пациентов, срочно нуждающихся в трансплантации
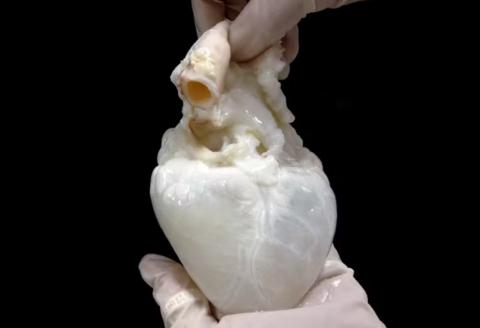
В США ежедневно умирают около 17 человек, ожидающих пересадки органов, — 6200 человек в год. А для более чем 10 000 американцев, ожидающих пересадки печени, будущее медицины может заключаться не в списке доноров, а в списке призраков.
Термин «орган-призрак» относится к биоинженерному процессу, при котором существующий орган аккуратно лишается всех своих собственных клеток. Остаётся лишь чистый, полупрозрачный белковый каркас — внеклеточный матрикс (ВКМ) — природный архитектурный проект органа. Затем каркас рецеллюляризируется, засеваясь либо новыми клетками пациента, либо здоровыми донорскими клетками, либо стволовыми клетками пациента — метод, который теоретически может быть использован для создания любого органа или ткани в организме человека.
Долгие годы цель технологии децеллюляризации/рецеллюляризации, позволяющей вырастить по требованию устойчивый к отторжению орган, казалась далёкой научной фантастикой. Но недавние прорывы сделали эту мечту реальностью.
В июне этого года компания Miromatrix Medical Inc. объявила о победе в первом клиническом испытании своего искусственного альтернативного органа. Система miroliverELAP, представляющая собой внешнее устройство для поддержки печени, состоит из децеллюляризированного каркаса из свиной печени, в который заселяются донорские клетки печени человека, создавая биоинженерную печень, функционирующую вне организма и обеспечивающую временную поддержку. Эта внешняя печеночная система является первой в своем роде, прошедшей клинические испытания на людях, она подключена через внешний кровеносный контур для воспроизведения основных функций здоровой печени.
Операция была успешно проведена в медицинском центре Intermountain в городе Мюррей, штат Юта, под руководством доктора Кристофера Дж. Дэнфорда , гепатолога-трансплантолога Intermountain Health. Пациент, которому была проведена пересадка печени, не подходил для трансплантации и страдал печёночной недостаточностью.
По словам Дэнфорда, внешняя печень, помещённая в контейнер, подвергалась перфузии в течение 48 часов, аналогично диализу, с целью проверки безопасности и эффективности. «Это было очень волнительно. Я опасался, не оторвётся ли этот тромб? Не вызовет ли это непредвиденных проблем?», — сказал Дэнфорд.
К счастью, непредвиденных проблем не возникло, и орган успешно выполнил важнейшие функции здоровой печени, предоставив один из самых ощутимых на сегодняшний день признаков того, что выращенные в лабораторных условиях и пригодные для трансплантации твердые человеческие органы могут стать реальным решением.
Набор участников в исследование первой фазы Miromatrix всё ещё открыт в восьми центрах США. Изначально исследование было открыто только для пациентов с острой печёночной недостаточностью, но затем оно было расширено и теперь включает острую печёночную недостаточность и алкогольный гепатит.
Основная идея технологии создания нового органа заключается в том, чтобы очистить ВКМ от исходных клеток и затем заселить этот естественный каркас новыми клетками. Собственная технологическая платформа Miromatrix основана на использовании децеллюляризированных органов свиньи. Их запатентованный процесс использует перфузионную децеллюляризацию и рецеллюляризацию, при которых все свиные клетки бережно удаляются из органа, оставляя сложную белковую структуру совершенно нетронутой.
По сути, орган-призрак — это каркас органа. Учёные обрабатывают орган серией мягких детергентов и ферментов, действующих подобно мылу, смывая весь клеточный материал, включая ДНК и всё, что может вызвать иммунное отторжение.
«Мы используем кровоснабжение этого органа, чтобы пропустить раствор, и поскольку кровоснабжение достигает каждой клетки, оно разрушает каждую клетку в органе, а затем можно вымыть всю эту клеточную слизь», — сказала Дорис А. Тейлор, соучредитель Miromatrix, которая теперь теперь сосредоточена на сердечно-сосудистой регенеративной медицине, совершенствуя процесс удаления/пересадки клеток для целых сердец.
После лизиса сердечных клеток и создания каркаса сердца туда вживляют индуцированные плюрипотентные стволовые клетки самого пациента. Эти стволовые клетки могут дифференцироваться в любой тип клеток человека, например, в гепатоциты печени, гладкомышечные клетки артерий и вен и кардиомиоциты сердца. Поскольку они получены от самого пациента, они создают персонализированный орган, который не будет отторгнут иммунной системой реципиента, что потенциально исключает необходимость пожизненного приема иммунодепрессантов.
Как только клетки посеяны, природа берет верх, получая правильный толчок от инженеров, создающих орган. «Матрица обучает клетки, что делать, если сначала мы перестроим сосудистое дерево, а затем добавим смесь соответствующих клеток сердечной мезодермы и распределим их по всему сердцу. Затем мы даём им правильные механические и электрические сигналы», — сказала Тейлор.
Последний этап — процесс созревания. Современные биореакторы имитируют работу человеческого организма, превращая эти пересаженные сердца в сильные, функциональные органы, способные поддерживать жизнь.
Вероятно, самым сложным аспектом в построении любого функционального цельного органа является перестройка всей сосудистой системы органа с помощью нового слоя эндотелиальных клеток, чтобы они могли созреть и справиться со всей рабочей нагрузкой живой ткани, поскольку это подразумевает одновременное решение двух монументальных проблем: предотвращение немедленного, катастрофического свертывания крови и восстановление сложных, жизненных функций сосудистой системы в массовом масштабе.
Эндотелиальные клетки, выстилающие сосуды, реагируют на кровоток и выделяют молекулы, регулирующие кровяное давление и воспаление. Напряжение сдвига, вызванное кровотоком, может повредить тонкую слизистую оболочку, что может привести к отёку, если она слишком проницаема.
Внеклеточный матрикс, обнажающийся после вымывания клеток, богат белками, такими как коллаген, но обладает высокой тромбогенностью. Он мгновенно даёт сигнал тромбоцитам о необходимости склеивания. Предотвращение тромбоза критически важно для предотвращения закупорки крупных сосудов, что может привести к кислородному голоданию органа и его гибели в течение нескольких минут или часов после трансплантации. По словам Тейлор, преимущество этих децеллюляризированных каркасов в том, что кровеносные сосуды в них сохраняются: «Это открывает путь к спасению жизней и начинает давать пациентам надежду, даёт врачам данные и даёт миру ощущение, что это уже не научная фантастика, а медицина».
Пока мечта о трансплантации твердых органов, таких как сердце и печень, выращенных из децеллюляризованных каркасов, остается на горизонте, одна компания воплотила эту технологию в жизнь, сосредоточившись на соединительной ткани: кровеносных сосудах.
Лора Никласон, доктор медицинских наук, основатель и генеральный директор Humacyte , профессор анестезиологии и биомедицинской инженерии в Йельском университете, внедряет новую технологию для людей с травматическими повреждениями, затрагивающими их кровеносную систему, создав сосуды из бесклеточной ткани. Сосуды создаются путём культивирования человеческих сосудистых клеток на биоразлагаемом трубчатом каркасе в биореакторе, обеспечивающем естественную механическую стимуляцию, необходимую для жизнеспособности сосуда. После того, как клетки образуют прочный естественный матрикс, их аккуратно смывают, оставляя прочный, готовый к использованию сосуд-«призрак», который универсально имплантируется и устойчив к инфекциям.
«Мы выращиваем сосуды в биореакторных мешках. Каждый мешок содержит один сосуд. Длина сосуда составляет 42 см, а диаметр — 6 мм… Затем мы децеллюляризуем его в мешке и отправляем на хранение в больницу до тех пор, пока его не откроет хирург», — сказала Никласон.
В настоящее время сосуды одобрены FDA для лечения травматических повреждений, например, у пациентов с сосудистыми повреждениями в результате автомобильных аварий или огнестрельных ранений. Но их потенциальные показания могут быть шире, например, для пациентов с заболеваниями периферических сосудов. Пациенты с закупоркой артерий ног страдают ишемией нижних конечностей и нуждаются в реваскуляризации, которая, по словам Никласон, показала «действительно обнадеживающие результаты в клинических испытаниях». Ещё одно потенциальное показание — пациенты с почечной недостаточностью, находящиеся на диализе.
Чтобы гарантировать, что процесс децеллюляризации в кровеносных сосудах не повреждает важные компоненты ВКМ, компания использует набор анализов для контроля качества, включая тест на прочность удержания шва и прочность на разрыв, чтобы убедиться, что материал способен выдерживать постоянное давление артериальной крови без протечек или разрывов. В дополнение ко всему этому, проводится количественная протеомика для проверки молекул матрикса и подтверждения регенеративного потенциала.
Что касается первой успешной трансплантации выращенного в лаборатории цельного органа, то это может быть гораздо ближе, чем мы думаем. «Ведётся масштабная работа с лёгкими, сердцем, печенью и почками», — сказала Тейлор. - Сейчас у нас есть технологии, позволяющие в течение 5 лет провести первую трансплантацию сердца человеку, если у нас будет достаточно финансирования. Всё дело в нем».
Игорь НАУМОВ
По материалам Medscape

Издательский отдел: +7 (495) 608-85-44 Реклама: +7 (495) 608-85-44,
E-mail: mg-podpiska@mail.ru Е-mail rekmedic@mgzt.ru
Отдел информации Справки: 8 (495) 608-86-95
E-mail: inform@mgzt.ru E-mail: mggazeta@mgzt.ru





